Билирубин
и его фракции
КОГДА ВАЖНО
ОПРЕДЕЛЕНИЕ БИЛИРУБИНА В СЫВОРОТКЕ КРОВИ
Определение билирубина в сыворотке крови используется для:
· постановки диагноза – гепатит на ранней стадии, цирроз, жировое перерождение, алкогольная болезнь печеночной ткани, раковая опухоль печени или метастазы, врожденные нарушения обмена билирубина;
· выявления ускоренного разрушения эритроцитов при гемолитической анемии (врожденные, аутоиммунные или токсические, после переливания крови);
· дифференциальной диагностики (отличия) физиологической (естественной) желтухи новорожденного от опасной ядерной энцефалопатии (избыток билирубина откладывается в ядрах головного мозга);
· выяснения степени закупорки желчных путей при наличии камня, опухоли или воспаления с нарушением оттока желчи;
· контроля за лечением болезней печени, крови и желчевыводящей системы;
· оценки повреждающего действия медикаментов.
Схема обмена билирубина
СИМПТОМЫ, ПРИ КОТОРЫХ
НУЖНО ПРОЙТИ АНАЛИЗ:
- пожелтение кожи;
- упорный зуд кожных покровов;
- потемнение мочи;
- слабость и утомляемость, ломота в костях, суставах в сочетании с болью, тяжестью в правом подреберье.
ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ ПОКАЗАТЕЛЯ
Показатель
билирубина имеет диагностическое значение при:
· ускоренном гемолизе (разрушении эритроцитов) на фоне анемии, малярии, заражении крови (сепсис);
· повреждении печени вирусом, алкоголем, ядом – гепатите;
·
гнойнике в печеночной
ткани (абсцесс);
·
замещении разрушенной
ткани рубцовыми волокнами – цирроз;
·
опухолевом процессе в
печени (первичный рак) или метастазировании из других органов;
·
подпеченочной
закупорке желчных путей – желчнокаменная болезнь, опухоль поджелудочной железы
или панкреатит, холангит, холецистит.
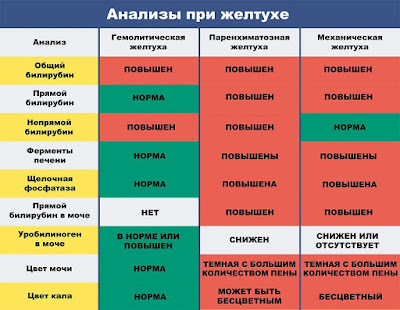
Все эти
болезни протекают с повышением общего билирубина, но его фракции (прямая и
непрямая часть) растут в разной степени. Поэтому исследование
помогает отличить вид желтухи:
·
надпеченочная
(гемолитическая),
·
внутрипеченочная
(паренхиматозная),
·
подпеченочная
(механическая).
Снижение билирубина имеет низкое диагностическое значение и
встречается при нарушении правил проведения анализа (употребление алкоголя,
кофе, снотворных, антибиотиков, гормонов, противосудорожных). Причиной низких
показателей бывает и нахождение в светлом месте сыворотки из венозной крови.
МЕТОДЫ ОПРЕДЕЛЕНИЯ
БИЛИРУБИНА В СЫВОРОТКЕ КРОВИ
Одного
рекомендованного метода (референсного) для определения билирубина в сыворотке
крови нет, в разных лабораториях могут использовать такие способы:
Для исследования общего билирубина
и его фракций применяются:
1. Прямые спектрофотометрические методы,
основаны на измерении абсорбции билирубина при 440‑460 нм, источником ошибок
здесь является интерференция желтых небилирубиновых пигментов;
2. Ферментативные методы,
основаны на окислении пигмента медьсодержащим ферментом билирубиноксидазой (КФ
1.3.3.5.), с образованием биливердина и исчезновением абсорбции при 460 нм.
Методы этой группы точны и отличаются высокой специфичностью и
чувствительностью;
3. Колориметрические диазометоды,
базируются на взаимодействии билирубина с диазотированной сульфаниловой
кислотой с образованием азопигментов. Под воздействием кислоты разрывается
тетрапирроловая структура билирубина с образованием двух дипирролов, углеродные
атомы метиленовых групп вступают в прямую реакцию с диазотированной сульфоновой
кислотой (диазосмесь) с образованием розово-фиолетовых изомеров азодипиррола с
максимумом поглощения при 530 нм. Связанный билирубин реагирует быстро,
несвязанный –– только после добавления акселератора (кофеин, метанол, мочевина,
бензоат или гидроокись натрия, уксусная кислота и другие). Последний
освобождает билирубин из комплекса с белками и тем самым ускоряет реакцию
азосочетания. Образовавшийся азокраситель ведет себя как кислотно-основной
индикатор с несколькими цветными переходами: в сильнокислой среде он окрашен в
фиолетовый цвет, в слабощелочной и слабокислой — в розовый, в сильнощелочной
среде — в синий или зеленый цвета.
4. Электрохимические методы
с использованием платинового и ртутного электродов;
5. Хроматографическое разделение
отдельных фракций билирубина;
6. Флюорометрические методы,
используется свойство свободного билирубина после поглощения при 430 нм
испускать свет длиной 520 нм. Позволяют определить концентрацию
неконъюгированного билирубина и, после обработки детергентом, общего билирубина
главным преимуществом метода является возможность использовать микроколичества
сыворотки.
Унифицированным методом
определения количества билирубина в сыворотке является метод Йендрашика‑Клеггорна‑Грофа
по диазореакции в щелочной или слабокислой среде в присутствии акселератора.
ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ БИЛИРУБИНА И
ЕГО ФРАКЦИЙ
В СЫВОРОТКЕ КРОВИ ПО ДИАЗОРЕАКЦИИ
ПРИНЦИП
Билирубин взаимодействует с диазотированной сульфоновой кислотой в присутствии кофеина с образованием окрашенных азопигментов.
Нормальные величины
ВЛИЯЮЩИЕ ФАКТОРЫ
Завышенные результаты вызывает гемолиз, прием стероидных препаратов,
эритромицина, фенобарбитала, употребление пищи, содержащей каротиноиды
(морковь, абрикосы). Длительное стояние сыворотки на свету вызывает окисление
билирубина и занижает значения.
КЛИНИКО‑ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ
Сыворотка
Накопление
билирубина в крови свыше 43 мкмоль/л ведет к связыванию его эластическими
волокнами кожи и конъюктивы, что проявляется в виде желтухи. Для
дифференциальной диагностики желтух необходимо определить, за счет какой
фракции возникает билирубинемия:
1. Гемолитическая или
надпеченочная желтуха — ускоренное образование билирубина в результате внутрисосудистого
гемолиза. Это гемолитические анемии различного происхождения: отравление
сульфаниламидами,талассемии, сепсис, лучевая болезнь, несовместимость крови,
врожденный сфероцитоз, серповидно-клеточная анемия, дефицит
глюкозо-6-фосфатдегидрогеназы.
В данном
случае гипербилирубинемия развивается
за счет фракции непрямого
билирубина. Гепатоциты усиленно переводят непрямой билирубин
в связанную форму, секретируют его в желчь, в результате в кале увеличивается
содержание стеркобилина,
интенсивно его окрашивая. В моче резко возрастает содержание уробилина, билирубин отсутствует.
У новорожденных
гемолитическая желтуха может развиться как симптом гемолитической болезни
новорожденного.
2. Паренхиматозная (печеночно-клеточная)
желтуха – причиной может быть нарушение на всех стадиях превращения билирубина
в печени: извлечение билирубина из крови печеночными клетками, его
конъюгирование и секреция в желчь. Наблюдается при вирусных и других формах
гепатитов, циррозе и опухолях печени, жировой дистрофии, при отравлении
токсическими гепатотропными веществами, при врожденных патологиях.
Так как в печени
недостаточно проходят все реакции превращения билирубина, гипербилирубинемия
развивается за счет обеих фракций,
преимущественно фракции прямого билирубина. Количество непрямого билирубина возрастает за
счет функциональной недостаточности гепатоцитов и/или снижения их количества,
а прямого — за
счет увеличения проницаемости мембран клеток печени, также из-за нарушения
секреции в желчь.
В моче
определяется билирубин (цвет
крепкого черного чая), умеренно увеличена концентрация уробилина, уровень стеркобилина кала в норме или
снижен.
У младенцев
вариантами паренхиматозной желтухи являются желтухи новорожденных и недоношенных: физиологическая
желтуха, желтуха, вызываемая молоком матери, и т.п.. Наследственные желтухи печеночного происхождения представляют
собой синдромы Жильбера-Мейленграхта, Дубина-Джонсона, Криглера-Найяра.
3. Механическая или
подпеченочная желтуха развивается вследствие нарушения оттока желчи при
закупорке желчного протока – желчные камни, новообразования поджелудочной железы,
гельминтозы. Также подпеченочные желтухи выявляются при новообразованиях
поджелудочной железы и гельминтозах.
В
результате застоя желчи происходит растяжение желчных капилляров, увеличивается
проницаемость их стенок. Не имеющий оттока в желчь прямой билирубин поступает в кровь и
развивается гипербилирубинемия за счет увеличения
концентрации прямого билирубина. В моче резко увеличен
уровень билирубина (цвет темного пива) и снижено
количество уробилина, в кале практически отсутствует стеркобилин (серовато-белое
окрашивание).
В
тяжелых случаях, вследствие переполнения гепатоцитов прямым билирубином,
конъюгация его с глюкуроновой кислотой может нарушаться и в крови будет
увеличиваться количество несвязанного билирубина, т.е. присоединяется печеночно-клеточная желтуха.
Моча
Закупорка
внепеченочных желчных путей является классической причиной билирубинурии.
Показатель полезен в дифференциальной диагностике желтух, поскольку
билирубинурия характерна для обтурационной и паренхиматозной желтух (повышение
уровня связанного билирубина в сыворотке), но отсутствует при гемолитической.
При гепатите билирубин может быть обнаружен в моче до появления желтухи.
Амниотическая жидкость
Билирубин
содержится почти исключительно в неэтерифицированном виде в комплексе с альбумином
и накапливается при эритробластозе, инфекционном гепатите и серповидноклеточном
кризе у матери.
ЛАБОРАТОРНАЯ РАБОТА
Принцип метода. Связанный билирубин при взаимодействии с диазореактивом (диазофенилсульфоновая кислота) образует розовое окрашивание, интенсивность которого пропорциональна концентрации билирубина, вступающего в прямую реакцию. Кофеиновый реактив переводит несвязанный билирубин в растворимое состояние, благодаря чему он также реагирует с диазореактивом, образуя розовое окрашивание. По интенсивности этого суммарного окрашивания определяют концентрацию общего билирубина. А концентрацию не связанного билирубина определяют, как разность между общим и связанным билирубином.
Ход работы. В 3 пробирки приливают реактивы по схеме:
Через 5-10 мин после прибавления диазореактива колориметрируют пробу на связанный билирубин (при более длительном стоянии пробы в реакцию вступает несвязанный билирубин, что искажает результат). Пробу на общий билирубин колориметрируют через 20 мин после добавления диазореактива. Колориметрирование проводят при зеленом светофильтре в кювете толщиной 0,5 см против контроля. Концентрацию общего и связанного билирубина определяют по калибровочному графику.
Нормальное содержание билирубина в сыворотке: общий –
1,7-20,5 ммоль/л, связанный – 0,86-4,3 мкмоль/л, свободный – 1,7-17,1 мкмоль/л.
Диагностическое значение определения билирубина в сыворотке крови.
Причины, вызывающие гипербилирубинемию, различны.
Желтуха появляется, когда уровень билирубина в крови превышает 43 мкмоль/л.
Заболевания, вызывающие повышение связанного билирубина: вирусный гепатит,
цирроз печени, опухоль печени и метастазы, жировая дистрофия.
Заболевания,
вызывающие повышение несвязанного билирубина: гемолитическая анемия,
пернециозная анемия, желтуха новорожденных.
Вопросы к защите лабораторной работы:
1. Объясните термины: общий билирубин, свободный билирубин, связанный билирубин, прямой билирубин, непрямой билирубин, конъюгированный билирубин, неконъюгированный билирубин.
2. Как образуется свободный билирубин?
3. Зачем в данном методе используется кофеиновый реактив?
4. Почему пробу на связанный билирубин колориметрируют точно через 5-10 минут?
5. Каков принцип метода определения билирубина в сыворотке крови?
6. Как определяют концентрацию общего и связанного билирубина?
7. Назовите причины гипербилирубинемии.
8. Какова норма свободного, связанного и общего билирубина?